Hóa học - Axit, bazơ và muối
Giới thiệu
Chúng ta nếm thức ăn chua và đắng, đó chỉ là do sự hiện diện của axit và bazơ tương ứng.
Giải pháp Litmus
Litmus, được chiết xuất từ địa y, có màu tím (xem hình ảnh bên dưới), nhưng điều kiện là khi nó không có tính axit hoặc bazơ, tức là trung tính.

Về cơ bản, cây quỳ là một loài thực vật thuộc họ Thallophyta, và trong thí nghiệm hóa học, nó thường được dùng làm chất chỉ thị.
Các chất thay đổi mùi trong môi trường axit hoặc bazơ, được gọi là olfactory các chỉ số.
Axit hoặc bazơ trong dung dịch nước
Các ion hydro trong HCl được tạo ra do sự có mặt của nước. Thứ hai, việc tách ion H + ra khỏi phân tử HCl không thể thực hiện được trong điều kiện không có nước. Công thức hóa học được minh họa bên dưới
HCl + H2O → H3O+ + Cl–
Hơn nữa, các ion hydro không thể tồn tại một mình, nhưng chúng có thể tồn tại khi có mặt các phân tử nước. Do đó, các ion hydro được hiển thị dưới dạng H + (aq) hoặc ion hydronium (H 3 O + ). Công thức hóa học là -
H+ + H2O → H3O+
Các bazơ hòa tan trong nước được gọi là alkalis. Nhưng tất cả các bazơ đều không tan trong nước.
Nếu cho nước vào axit đậm đặc thì nhiệt lượng được sinh ra.
Trộn axit hoặc bazơ với nước làm giảm nồng độ của các ion (tức là H 3 O + / OH–) trên một đơn vị thể tích và quá trình này được gọi làdilution.
quy mô ph
Một thang đo, được sử dụng để đo nồng độ ion hydro trong dung dịch, được gọi là pH scale.
Các ‘p’ trong pH là viết tắt của ‘potenz’, nó là một thuật ngữ tiếng Đức, có nghĩa là ‘power’.
Giá trị pH được lấy đơn giản là một con số, cho biết tính chất axit hoặc bazơ của dung dịch. Vì vậy, nếu nồng độ của ion hydronium cao hơn, thì giá trị của pH sẽ thấp hơn.
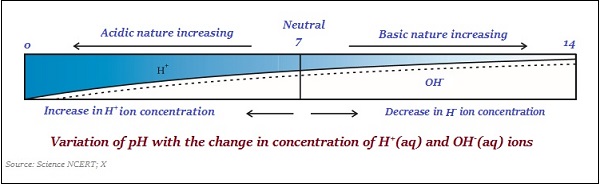
Giá trị của thang pH nằm trong khoảng giữa ‘0’ và ’14;’ vì vậy, nếu giá trị pH được đo bằng '0', điều đó có nghĩa là - nó rất acidic và nếu nó là 14, thì nó có nghĩa là - nó rất alkaline.
Giá trị trung tính của thang pH là ‘7’.
Trên thang đo pH, giá trị nhỏ hơn 7 thể hiện dung dịch có tính axit và giá trị lớn hơn 7 thể hiện dung dịch bazơ.
Thông thường, giấy tẩm chất chỉ thị thông thường được sử dụng để đo độ pH (xem hình ảnh bên dưới) -
Tương tự như vậy, độ mạnh của chất axit và bazơ chủ yếu phụ thuộc vào số lượng ion H + và ion OH - được tạo ra tương ứng.
Hình ảnh sau đây minh họa khái quát (các biến thể về màu sắc) giá trị pH của một số chất phổ biến -

Tầm quan trọng của pH trong cuộc sống hàng ngày
Giá trị pH của cơ thể con người nằm trong khoảng từ 7,0 đến 7,8.
Dạ dày của cơ thể con người sản xuất axit clohydric giúp tiêu hóa thức ăn; đáng ngạc nhiên là dù sao nó cũng không gây hại cho dạ dày.
Tuy nhiên, khi dạ dày tạo ra quá nhiều axit (được gọi là khó tiêu), nó sẽ gây ra đau và kích thích. Để giảm cơn đau này, các bác sĩ khuyên bạn nên sử dụng các chất nền được gọi là thuốc kháng axit.
Các thuốc kháng axit này trung hòa và kiểm soát lượng axit tăng lên.
Răng, được tạo thành từ canxi photphat, là chất cứng nhất trong cơ thể. Tuy nhiên, khi độ pH trong miệng giảm xuống (dưới 5,5), nó sẽ ăn mòn răng.
Thông thường, muối được tạo thành do sự kết hợp của axit clohydric và dung dịch natri hydroxit; và, sự kết hợp được gọi là natri clorua.
Khi giá trị pH của nước mưa được đo nhỏ hơn 5,6, nó được gọi là acid rain.
Khi mưa axit chảy vào sông, nó cũng làm giảm độ pH của nước sông
Nước sông có tính axit là mối đe dọa cho sự tồn tại của các loài thủy sinh.
Bột tẩy trắng
Bột tẩy trắng được tạo ra do tác dụng của clo với vôi tôi [Ca (OH) 2 ] khô và nó được đại diện là CaOCl 2 .
Bột tẩy trắng thường được sử dụng trong ngành dệt may, nhà máy giấy, công nghiệp hóa chất và khử trùng nước uống.
Baking Soda
Baking soda thường được sử dụng trong nhà bếp để nấu các món ăn giòn ngon. Nó cũng nấu một số món ăn nhanh hơn.
Tên hóa học của muối nở là natri hiđrocacbonat và công thức là NaHCO 3 .
Soda rửa
Kết tinh lại của natri cacbonat thành soda giặt.
Công thức hóa học của soda wash là Na 2 CO 3 .10H 2 O.
Soda rửa được sử dụng phổ biến trong các ngành sản xuất thủy tinh, xà phòng và giấy.
Thạch cao Paris
Plaster of Paris là một loại bột màu trắng mà các bác sĩ sử dụng làm thạch cao để hỗ trợ xương bị gãy.
Tên hóa học của thạch cao của paris là canxi sulfat hemihydrate và công thức hóa học là 2CaSO 4 .H 2 O.