Química - Carbono
Introducción
El carbono es un elemento tetravalente y no metálico.
Medios tetravalentes: el carbono hace que cuatro electrones estén disponibles para formar los enlaces químicos covalentes.
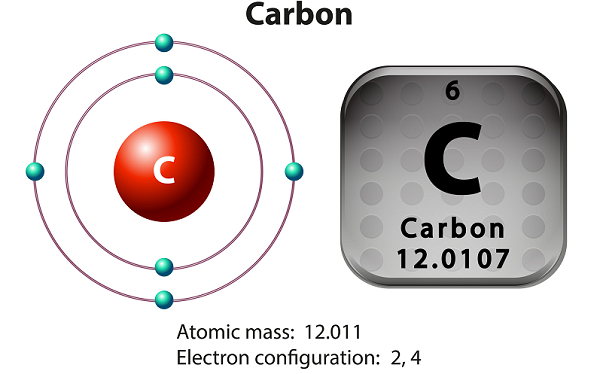
El carbono tiene tres isótopos que se producen naturalmente, a saber, 12 C, 13 C y 14 C.
Entre ellos, el 12 C y el 13 C son estables, pero el 14 C es un isótopo radiactivo. La vida media del 14 C es de aproximadamente 5.730 años.
Características destacadas del carbono
Las propiedades físicas del carbono dependen en gran medida de sus alótropos.
Los principales alótropos del carbono son el grafito, el diamante y el carbono amorfo.
El grafito es opaco, negro y muy suave; por lo tanto, solía formar una raya en el papel.
Diamante muy duro (el material natural más duro) y transparente.
El grafito es un buen conductor de electricidad.
El diamante es un mal conductor de la electricidad.
Lo más probable es que el carbono tenga el punto de sublimación más alto entre todos los elementos.
Aparición de carbono
En términos de masa, el carbono es el cuarto elemento químico más abundante que se encuentra en el universo (después del hidrógeno, el helio y el oxígeno).
El carbono está disponible en abundancia en el Sol, las estrellas, los cometas y en las atmósferas de la mayoría de los planetas.
El carbono se encuentra en la atmósfera terrestre y se disuelve en agua.
Los hidrocarburos, como el carbón, el petróleo y el gas natural, todos contienen carbono.
El carbono también se encuentra en los hidratos de metano, que se encuentran en las regiones polares y bajo los mares.
Algunas de las rocas enriquecidas en carbono son carbón, caliza, dolomita, etc.
El carbón es muy rico en carbono; por tanto, es la mayor fuente comercial de carbono mineral.
El carbón comparte alrededor de 4.000 gigatoneladas o el 80% del total de combustibles fósiles.
Compuestos de carbono
Los siguientes son los principales compuestos de carbono:
Cianógeno - CN 2
Cianuro de hidrógeno - HCN
Cianamida - CN 2 H 2
Ácido isociánico - HNCO
Cloruro de cianógeno - CNCl
Isocianato de clorosulfonilo - CNClO 3 S
Cloruro cianúrico - NCCl 3
Disulfuro de carbono - CS 2
Sulfuro de carbonilo - OCS
Monosulfuro de carbono - CS
Usos del carbono
Dependiendo de las alótropas, el carbono se utiliza en una variedad de aplicaciones.
El carbono es uno de los elementos más esenciales de la vida sin él, no podemos imaginar la vida en la tierra.
Los combustibles fósiles, a saber, gas metano y petróleo crudo (petróleo), carbón, etc., se utilizan en la vida cotidiana.
Grafito, combinado con arcilla, utilizado en la fabricación de "plomo" utilizado en lápices.
El carbón vegetal también se utiliza como material de dibujo en obras de arte, fundición de hierro, parrillas de barbacoa, etc.
El diamante se usa generalmente en joyería.
Los diamantes industriales se utilizan en herramientas de corte, perforación y pulido para mecanizar metales y piedra.
Los hidrocarburos fósiles y la fibra de carbono se utilizan para fabricar plástico.