Química - Cálcio
Introdução
O cálcio é um elemento alcalino amarelo-acinzentado suave encontrado principalmente na crosta terrestre.
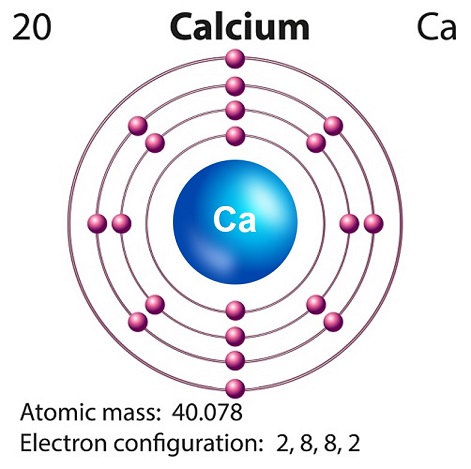
O símbolo do cálcio é “Ca” e o número atômico é “20.”
O cálcio livre quase não existe na natureza, pois é altamente reativo.
O cálcio é produzido geralmente na nucleossíntese de supernova.
Características salientes do cálcio
O cálcio é um dos metais mais abundantes em massa, encontrado em muitos animais.
O cálcio é um constituinte muito importante dos dentes, ossos e conchas.
O carbonato de cálcio e o citrato de cálcio são os principais suplementos dietéticos necessários para uma boa saúde.
A Organização Mundial da Saúde (OMS) listou o cálcio como medicamento essencial.
Em comparação com outros metais, o íon cálcio e a maioria dos outros compostos de cálcio têm baixa toxicidade.
Se o cálcio entrar em contato com água ou ácido, ele reage com eles e se torna perigoso.
Se o cálcio entrar em contato com o ar, ele reage rapidamente e forma uma camada cinza-esbranquiçada de nitreto de cálcio e óxido de cálcio.
A maioria dos sais de cálcio são normalmente incolores.
Quando o cálcio queima, a cor de sua chama parece vermelho tijolo (veja a imagem abaixo).

O metal de cálcio tem comparativamente uma resistividade elétrica mais alta do que o alumínio ou cobre.
Ocorrência
O cálcio ocorre geralmente em rochas sedimentares.
Os minerais (sedimentares) nos quais o cálcio é encontrado são calcita, dolomita e gesso.
O cálcio também é encontrado em rochas ígneas e metamórficas principalmente nos minerais silicatados, como anfibólios, plagioclásios, piroxênios e granadas.
O cálcio também é encontrado em muitos produtos alimentícios, como laticínios, amêndoas, avelãs, grãos de soja, brócolis, folhas de dente-de-leão, figos e em muitos mais.
Compostos de Cálcio
Óxido de cálcio - CaO
Hidróxido de cálcio - Ca (OH) 2
Cloreto de cálcio - CaCl 2
Hipoclorito de cálcio (pó clareador) - Ca (ClO) 2
Fosfato de cálcio - Ca 3 (PO 4 ) 2
Usos do cálcio
O cálcio tem uma ampla gama de uso, muitos deles são -
Carbonato de cálcio (CaCO 3 ) é usado na fabricação de cimento.
O carbonato de cálcio (CaCO 3 ) também é usado na fabricação de pasta de dente.
Em inseticidas, o arseniato de cálcio (Ca 3 (AsO 4 ) 2 ) é usado.
O cloreto de cálcio (CaCl 2 ) é usado na remoção de gelo e também no controle de poeira.
Citrato de cálcio (Ca 3 (C 6 H 5 O 7 ) 2 ) é comumente usado como conservante de alimentos.
O gluconato de cálcio (Ca (C 6 H 11 O 7 ) 2 ) é freqüentemente usado como aditivo alimentar, bem como em pílulas de vitaminas.
O hipoclorito de cálcio (Ca (OCl) 2 ) é geralmente usado como desinfetante de piscinas, como agente clareador.