Química - Urânio
Introdução
O urânio é o metal da série actinídeo da tabela periódica.
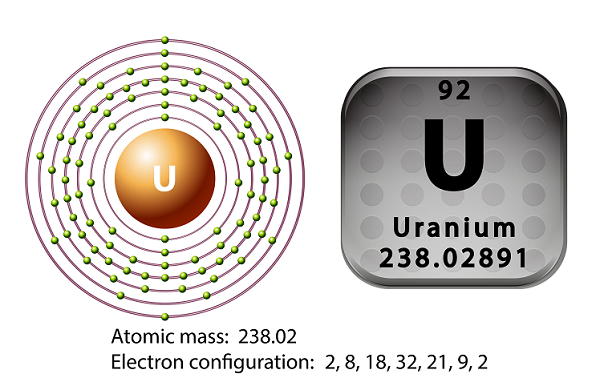
O símbolo do urânio é ‘U’ e o número atômico é ’92.’
Em 1789, Martin Heinrich Klaproth descobriu o elemento urânio e o batizou com o nome de Urano.
Características salientes do urânio
O urânio é um metal branco prateado.
Um átomo de urânio possui 92 elétrons, bem como 92 prótons, dos quais 6 são elétrons de valência.
Por ter isótopos instáveis, o urânio é um elemento radioativo fraco.
Urânio-238 é o isótopo mais comum de urânio.
O urânio ocorre naturalmente em concentrações muito baixas, ou seja, algumas partes por milhão na rocha, solo e água.
O urânio decai gradualmente (lentamente), emitindo sua partícula alfa.
O urânio tem baixa condutividade elétrica (mau condutor de eletricidade).
O urânio é maleável, dúctil e marginalmente paramagnético
Ocorrência de Urânio
O urânio é (naturalmente) encontrado como urânio-238, urânio-235 e urânio-234.
A meia-vida do urânio-238 é de cerca de 4,47 bilhões de anos, quase a idade da Terra, e a meia-vida do urânio-235 é de cerca de 704 milhões de anos.
Ligas de Urânio
A seguir estão as principais ligas de urânio -
Staballoy
Hidreto de urânio
Compostos de Urânio
A seguir estão os principais compostos de urânio -
Nitreto de urânio - U 2 N 3
Pentafluoreto de urânio - UF 5
Carboneto de urânio - UC
Fluoreto de uranila - UO 2 F 2
Dióxido de urânio - UO 2
Hexafluoreto de urânio - UF 6
Oxtoxido de triurânio - U 3 O 8
Tetrafluoreto de urânio - UF 4
Trióxido de urânio - UO 3
Tetracloreto de urânio - Ucl 4
Nitrato de uranil - UO 2 (NO 3 ) 2
Usos do Urânio
O urânio é usado como fonte de energia em submarinos nucleares (especialmente por militares).
O urânio é usado na fabricação de armas nucleares.
O urânio também é usado como reatores para navios.