เคมี - คาร์บอนและสารประกอบ
บทนำ
คาร์บอนมีบทบาทสำคัญมากสำหรับสิ่งมีชีวิตทุกชนิด
ปริมาณคาร์บอนในเปลือกโลกมีเพียง 0.02% ซึ่งมีอยู่ในรูปของแร่ธาตุเช่นคาร์บอเนตไฮโดรเจนคาร์บอเนตถ่านหินและปิโตรเลียม
การปรากฏตัวของคาร์บอนในบรรยากาศของโลกคือ 0.03% ในรูปของก๊าซคาร์บอนไดออกไซด์
สารประกอบของคาร์บอน
สารประกอบคาร์บอนเกือบทั้งหมด (ยกเว้นบางส่วน) เป็นตัวนำไฟฟ้าที่ไม่ดี
เพชรและกราไฟต์ทั้งคู่เกิดจากอะตอมของคาร์บอน อย่างไรก็ตามความแตกต่างอยู่ระหว่างพวกมันในลักษณะที่อะตอมของคาร์บอนยึดติดกัน
ในเพชรแต่ละอะตอมของคาร์บอนจะถูกผูกมัดกับคาร์บอนอีกสี่อะตอมและสร้างโครงสร้างสามมิติที่แข็ง (ดูภาพด้านล่าง)
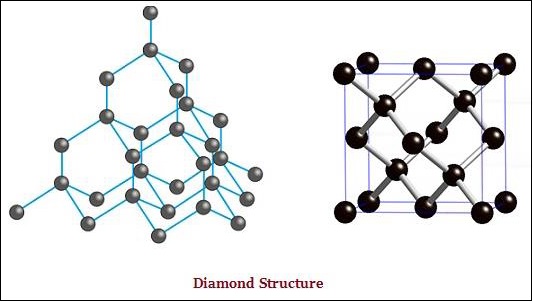
ในแกรไฟต์แต่ละอะตอมของคาร์บอนจะถูกผูกมัดกับคาร์บอนอีกสามอะตอมในระนาบเดียวกันซึ่งให้อาร์เรย์หกเหลี่ยม (ดูภาพด้านล่าง) -
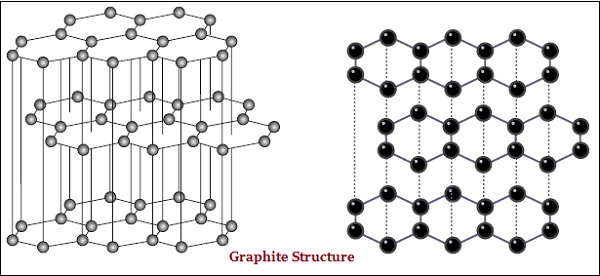
นอกจากนี้ยังมีความแตกต่างในโครงสร้างทางกายภาพของเพชรและกราไฟต์
เพชรเป็นสารที่แข็งที่สุดที่รู้จักในขณะที่กราไฟต์เป็นสารที่เรียบและลื่น
กราไฟท์เป็นตัวนำไฟฟ้าที่ดีในขณะที่เพชรไม่ใช่
ตารางต่อไปนี้แสดงโครงสร้างของสารประกอบคาร์บอนและไฮโดรเจน -
| ชื่อ | สูตร | โครงสร้าง |
|---|---|---|
| มีเทน | CH 4 |

|
| อีเทน | C 2 H 6 |

|
| โพรเพน | C 3 H 8 |

|
| บิวเทน | C 4 H 10 |

|
| เพนเทน | C 5 H 12 |

|
| เฮกเซน | C 6 H 14 |

|
สารประกอบที่มีสูตรโมเลกุลเหมือนกัน แต่มีโครงสร้างต่างกันเรียกว่า structural isomers (ดูโครงสร้างบิวเทนที่ระบุด้านล่าง)

ไฮโดรคาร์บอนอิ่มตัวเรียกว่า alkanes.
ไฮโดรคาร์บอนไม่อิ่มตัวซึ่งประกอบด้วยพันธะคู่หนึ่งพันธะหรือมากกว่านั้นเรียกว่า alkenes.
ไฮโดรคาร์บอนไม่อิ่มตัวซึ่งประกอบด้วยพันธะสามอย่างหนึ่งหรือมากกว่านั้นเรียกว่า alkynes.
การใช้แอลกอฮอล์เป็นเชื้อเพลิง
ต้นอ้อยเปลี่ยนแสงแดดเป็นพลังงานเคมีได้อย่างมีประสิทธิภาพและสามารถใช้น้ำผลไม้เพื่อเตรียมกากน้ำตาลได้
เมื่อหมักกากน้ำตาลจะทำให้เกิดแอลกอฮอล์ (เอทานอล)
ปัจจุบันบางประเทศใช้แอลกอฮอล์เป็นสารเติมแต่งในน้ำมันเนื่องจากเป็นเชื้อเพลิงที่สะอาดกว่า
แอลกอฮอล์เหล่านี้เมื่อเผาไหม้ในอากาศที่เพียงพอ (ออกซิเจน) จะทำให้เกิดก๊าซคาร์บอนไดออกไซด์และน้ำเท่านั้น
เอสเทอร์
เอสเทอร์เป็นสารที่มีกลิ่นหวานซึ่งส่วนใหญ่เกิดจากปฏิกิริยาของกรดและแอลกอฮอล์ (ดูภาพด้านล่าง - แสดงการก่อตัวของเอสเทอร์)
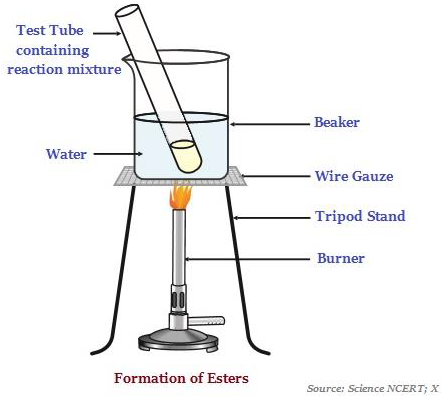
เมื่อเอสเทอร์ทำปฏิกิริยาต่อหน้ากรดหรือเบสจะให้แอลกอฮอล์และกรดคาร์บอกซิลิกกลับคืนมา
ปฏิกิริยาของเอสเทอร์กับกรดหรือเบสเรียกว่า saponification เพราะใช้ในการเตรียมสบู่
โมเลกุลของสบู่โดยปกติคือเกลือโซเดียมหรือโพแทสเซียมของกรดคาร์บอกซิลิกสายยาว
ที่น่าสนใจคือปลายไอออนิกของสบู่ละลายในน้ำในขณะที่โซ่คาร์บอนละลายในน้ำมัน คุณสมบัติทั่วไปของโมเลกุลสบู่นี้ก่อให้เกิดโครงสร้างที่เรียกว่าmicelles (ดูภาพด้านล่าง)

ในไมเซลล์ปลายด้านหนึ่งของโมเลกุลจะอยู่ตรงกับหยดน้ำมันในขณะที่ปลายไอออนิกยังคงอยู่ด้านนอก
ไมเซลล่าของสบู่ช่วยในการละลายสิ่งสกปรกในน้ำ ในทำนองเดียวกันเสื้อผ้าจะได้รับการทำความสะอาด
ในทางกลับกันผงซักฟอกมักเป็นแอมโมเนียมหรือเกลือซัลโฟเนตของกรดคาร์บอกซิลิกสายยาวซึ่งยังคงมีประสิทธิภาพแม้ในน้ำกระด้าง
โดยทั่วไปแล้วผงซักฟอกมักใช้ในการทำแชมพูและผลิตภัณฑ์อื่น ๆ สำหรับทำความสะอาดเสื้อผ้า