Chemie - Kalzium
Einführung
Calcium ist ein weiches grau-gelbes alkalisches Element, das hauptsächlich in der Erdkruste vorkommt.
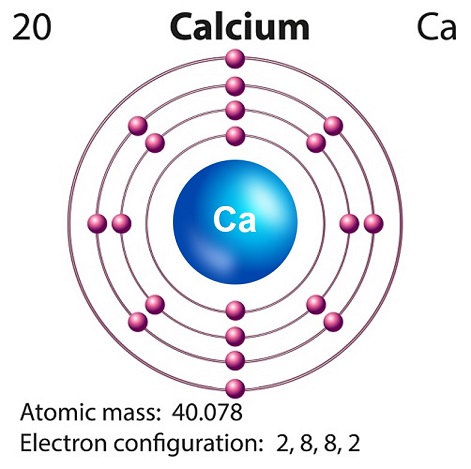
Das Symbol von Calcium ist “Ca” und Ordnungszahl ist “20.”
Freies Kalzium kommt in der Natur kaum vor, da es hochreaktiv ist.
Calcium wird normalerweise in der Supernova-Nukleosynthese hergestellt.
Hauptmerkmale von Kalzium
Calcium ist eines der am häufigsten vorkommenden Metalle bei vielen Tieren.
Calcium ist ein sehr wichtiger Bestandteil von Zähnen, Knochen und Muscheln.
Calciumcarbonat und Calciumcitrat sind die wichtigsten Nahrungsergänzungsmittel, die für eine gute Gesundheit erforderlich sind.
Die Weltgesundheitsorganisation (WHO) hat Kalzium als wesentliche Arzneimittel aufgeführt.
Im Vergleich zu anderen Metallen weisen das Calciumion und die meisten anderen Calciumverbindungen eine geringe Toxizität auf.
Wenn Kalzium mit Wasser oder Säure in Kontakt kommt, reagiert es mit ihnen und wird gefährlich.
Wenn Kalzium mit Luft in Kontakt kommt, reagiert es schnell und bildet eine grauweiße Beschichtung aus Kalziumnitrid und Kalziumoxid.
Die meisten Calciumsalze sind normalerweise farblos.
Wenn Kalzium verbrannt wird, erscheint die Farbe seiner Flamme ziegelrot (siehe das Bild unten).

Calciummetall hat einen vergleichsweise höheren spezifischen elektrischen Widerstand als Aluminium oder Kupfer.
Auftreten
Calcium kommt normalerweise in Sedimentgesteinen vor.
Die Mineralien (Sedimente), in denen Kalzium gefunden wird, sind Kalzit, Dolomit und Gips.
Calcium kommt auch in magmatischen und metamorphen Gesteinen vor, hauptsächlich in Silikatmineralien wie Amphibolen, Plagioklasen, Pyroxenen und Granaten.
Calcium kommt auch in vielen Lebensmitteln vor, nämlich Milchprodukten, Mandeln, Haselnüssen, Sojabohnen, Brokkoli, Löwenzahnblättern, Feigen und vielen anderen.
Calciumverbindungen
Calciumoxid - CaO
Calciumhydroxid - Ca (OH) 2
Calciumchlorid - CaCl 2
Calciumhypochlorit (Bleichpulver) - Ca (ClO) 2
Calciumphosphat - Ca 3 (PO 4 ) 2
Verwendung von Kalzium
Calcium hat ein breites Anwendungsspektrum, von denen bedeutende -
Calciumcarbonat (CaCO 3 ) wird zur Herstellung von Zement verwendet.
Calciumcarbonat (CaCO 3 ) wird auch zur Herstellung von Zahnpasta verwendet.
In Insektiziden wird Calciumarsenat (Ca 3 (AsO 4 ) 2 ) verwendet.
Calciumchlorid (CaCl 2 ) wird sowohl zur Eisentfernung als auch zur Staubbekämpfung eingesetzt.
Calciumcitrat (Ca 3 (C 6 H 5 O 7 ) 2 ) wird üblicherweise als Lebensmittelkonservierungsmittel verwendet.
Calciumgluconat (Ca (C 6 H 11 O 7 ) 2 ) wird häufig als Lebensmittelzusatzstoff sowie in Vitaminpillen verwendet.
Calciumhypochlorit (Ca (OCl) 2 ) wird im Allgemeinen als Schwimmbaddesinfektionsmittel, als Bleichmittel verwendet.