化学-カルシウム
前書き
カルシウムは、主に地球の地殻に見られる柔らかい灰色がかった黄色のアルカリ元素です。
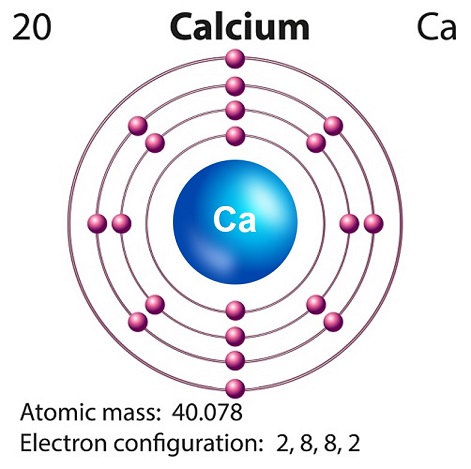
カルシウムのシンボルは “Ca” 原子番号は “20.”
遊離カルシウムは反応性が高いため、自然界にはほとんど存在しません。
カルシウムは通常、超新星元素合成で生成されます。
カルシウムの顕著な特徴
カルシウムは、多くの動物に見られる質量で最も豊富な金属の1つです。
カルシウムは、歯、骨、殻の非常に重要な成分です。
炭酸カルシウムとクエン酸カルシウムは、健康に必要な主要な栄養補助食品です。
世界保健機関(WHO)は、必須医薬品としてカルシウムを挙げています。
他の金属と比較して、カルシウムイオンと他のほとんどのカルシウム化合物は毒性が低いです。
カルシウムが水や酸と接触すると、それらと反応して危険になります。
カルシウムが空気と接触すると、カルシウムは迅速に反応し、窒化カルシウムと酸化カルシウムの灰白色のコーティングを形成します。
ほとんどのカルシウム塩は通常無色です。
カルシウムが燃焼すると、炎の色が赤レンガ色になります(下の画像を参照)。

金属カルシウムは、アルミニウムや銅よりも電気抵抗率が比較的高くなっています。
発生
カルシウムは通常、堆積岩で発生します。
カルシウムが見つかった鉱物(堆積物)は、方解石、苦灰石、石膏です。
カルシウムは、角閃石、斜長石、輝石、ガーネットなどのケイ酸塩鉱物に含まれる火成岩や変成岩にも含まれています。
カルシウムは、乳製品、アーモンド、ヘーゼルナッツ、大豆、ブロッコリー、タンポポの葉、イチジクなど、多くの食品にも含まれています。
カルシウムの化合物
酸化カルシウム- のCaO
水酸化カルシウム- のCa(OH)2
塩化カルシウム- のCaCl 2
次亜塩素酸カルシウム(漂白パウダー)- カルシウム(のClO)2
リン酸カルシウム- のCa 3(PO 4)2
カルシウムの使用
カルシウムには幅広い用途があり、その重要なものは次のとおりです。
炭酸カルシウム(CaCO 3)はセメントの製造に使用されます。
炭酸カルシウム(CaCO 3)は歯磨き粉の製造にも使用されます。
殺虫剤では、ヒ化カルシウム(Ca 3(AsO 4)2)が使用されます。
塩化カルシウム(CaCl 2)は、除氷や防塵に使用されます。
クエン酸カルシウム(Ca 3(C 6 H 5 O 7)2)は一般的に食品防腐剤として使用されます。
グルコン酸カルシウム(Ca(C 6 H 11 O 7)2)は、食品添加物としてだけでなく、ビタミン剤としても頻繁に使用されます。
次亜塩素酸カルシウム(Ca(OCl)2)は、一般的にプールの消毒剤、漂白剤として使用されます。