Química - Carbono e seus compostos
Introdução
O carbono desempenha um papel muito importante para todos os seres vivos.
A quantidade de carbono na crosta terrestre é de apenas 0,02%, disponível na forma de minerais como carbonatos, hidrogenocarbonatos, carvão e petróleo.
A presença de carbono na atmosfera terrestre é de 0,03%, na forma de dióxido de carbono.
Compostos de Carbono
Quase todos os compostos de carbono (exceto alguns) são maus condutores de eletricidade.
O diamante e a grafite são formados por átomos de carbono; no entanto, a diferença está entre eles na maneira como os átomos de carbono estão ligados uns aos outros.
No diamante, cada átomo de carbono está ligado a quatro outros átomos de carbono e forma uma estrutura tridimensional rígida (veja a imagem abaixo).
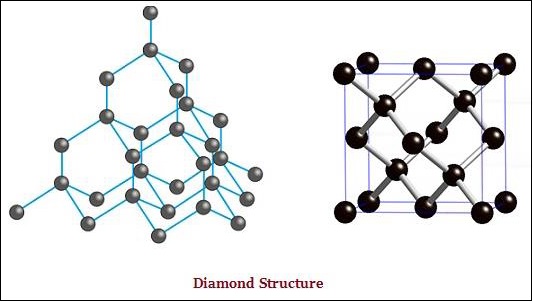
Na grafite, cada átomo de carbono está ligado a três outros átomos de carbono no mesmo plano, o que dá uma matriz hexagonal (veja a imagem abaixo) -
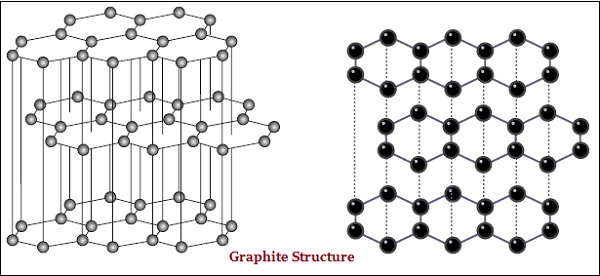
Também há diferença em algumas estruturas físicas de diamante e grafite.
O diamante é a substância mais dura conhecida, enquanto a grafite é uma substância lisa e escorregadia.
O grafite é um bom condutor de eletricidade, enquanto o diamante não.
A tabela a seguir ilustra as estruturas de compostos de carbono e hidrogênio -
| Nome | Fórmula | Estrutura |
|---|---|---|
| Metano | CH 4 |

|
| Etano | C 2 H 6 |

|
| Propano | C 3 H 8 |

|
| Butano | C 4 H 10 |

|
| Pentano | C 5 H 12 |

|
| Hexano | C 6 H 14 |

|
Os compostos, que possuem fórmula molecular idêntica, mas estruturas diferentes, são conhecidos como structural isomers (veja a estrutura Butano fornecida abaixo).

Os hidrocarbonetos saturados são conhecidos como alkanes.
Os hidrocarbonetos insaturados, que compreendem uma ou mais ligações duplas, são conhecidos como alkenes.
Os hidrocarbonetos insaturados, que compreendem uma ou mais ligações triplas, são conhecidos como alkynes.
Uso de álcool como combustível
As plantas de cana-de-açúcar muito eficientes convertem a luz solar em energia química e seu caldo pode ser usado para preparar melaço.
Quando o melaço é fermentado, ele produz álcool (etanol).
Alguns países já utilizam o álcool como aditivo na gasolina, por se tratar de um combustível mais limpo.
Esse álcool, ao ser queimado em ar suficiente (oxigênio), dá origem apenas a dióxido de carbono e água.
Ésteres
Ésteres são substâncias com cheiro doce, que são mais comumente formadas pela reação de um ácido e um álcool (veja a imagem abaixo - ilustrando a formação de ésteres).
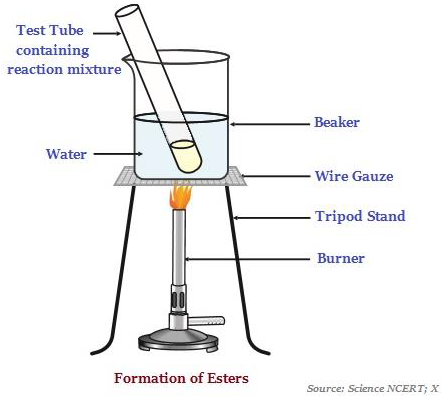
Quando os ésteres reagem na presença de um ácido ou base, ele retorna o álcool e o ácido carboxílico.
A reação de ésteres com um ácido ou uma base, é conhecida como saponification porque é usado na preparação de sabonetes.
As moléculas de sabão normalmente são sais de sódio ou potássio de ácidos carboxílicos de cadeia longa.
Curiosamente, a extremidade iônica do sabão se dissolve na água, enquanto a cadeia de carbono se dissolve no óleo. Essas características típicas das moléculas de sabão formam estruturas conhecidas comomicelles (veja a imagem abaixo)

Nas micelas, uma extremidade das moléculas está em direção à gota de óleo, enquanto a extremidade iônica permanece do lado de fora.
A micela de sabão ajuda a dissolver a sujeira na água; da mesma forma, as roupas são limpas.
Por outro lado, os detergentes são geralmente sais de amônio ou sulfonato de ácidos carboxílicos de cadeia longa, que permanecem eficazes mesmo em água dura.
Os detergentes costumam ser usados para fazer xampus e alguns outros produtos para limpar roupas.