Kimya - Karbon ve Bileşikleri
Giriş
Karbon, tüm canlılar için çok önemli roller oynar.
Yerkabuğundaki karbon miktarı yalnızca% 0,02'dir ve karbonatlar, hidrojen-karbonatlar, kömür ve petrol gibi mineraller şeklinde bulunur.
Dünya atmosferindeki karbon varlığı, karbondioksit formunda% 0,03'tür.
Karbon Bileşikleri
Hemen hemen tüm karbon bileşikleri (birkaçı dışında) elektriğin zayıf iletkenleridir.
Elmas ve grafit, karbon atomlarından oluşur; ancak, aralarındaki fark, karbon atomlarının birbirine bağlanma biçiminde yatmaktadır.
Elmasta, karbonun her bir atomu diğer dört karbon atomuna bağlanır ve sert bir üç boyutlu yapı oluşturur (aşağıdaki resme bakın).
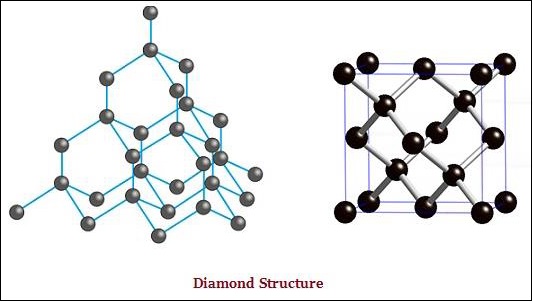
Grafitte, karbonun her bir atomu, aynı düzlemdeki diğer üç karbon atomuna bağlanır ve bu da altıgen bir dizi verir (aşağıdaki resme bakın) -
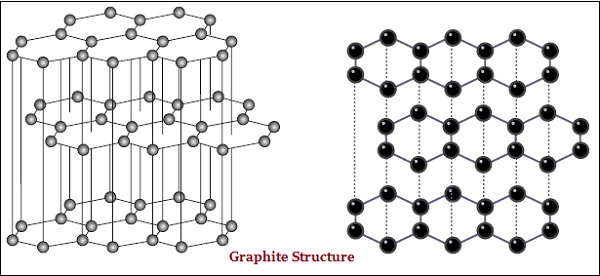
Elmas ve grafitin bazı fiziksel yapılarında da farklılık vardır.
Elmas bilinen en sert maddedir, grafit ise pürüzsüz ve kaygan maddedir.
Grafit iyi bir elektrik iletkenidir, oysa elmas değildir.
Aşağıdaki tablo, karbon ve hidrojen bileşiklerinin yapılarını göstermektedir -
| İsim | Formül | Yapısı |
|---|---|---|
| Metan | CH 4 |

|
| Etan | C 2 H 6 |

|
| Propan | C 3 H 8 |

|
| Bütan | C 4 H 10 |

|
| Pentan | C 5 H 12 |

|
| Hekzan | C 6 H 14 |

|
Aynı moleküler formüle sahip, ancak farklı yapılara sahip bileşikler, structural isomers (aşağıda verilen Bütan yapısına bakın).

Doymuş hidrokarbonlar şu şekilde bilinir: alkanes.
Bir veya daha fazla çift bağ içeren doymamış hidrokarbonlar, alkenes.
Bir veya daha fazla üçlü bağdan oluşan doymamış hidrokarbonlar, alkynes.
Alkolün Yakıt Olarak Kullanılması
Şeker kamışı bitkileri çok verimli bir şekilde güneş ışığını kimyasal enerjiye dönüştürür ve suyu pekmez hazırlamak için kullanılabilir.
Pekmez fermente edildiğinde alkol (etanol) üretir.
Bazı ülkeler artık daha temiz bir yakıt olduğu için benzinde katkı maddesi olarak alkol kullanıyor.
Bu alkol, yeterli havada (oksijen) yandığında sadece karbondioksit ve su açığa çıkarır.
Esterler
Esterler, en yaygın olarak bir asit ve bir alkolün reaksiyonu sonucu oluşan tatlı kokulu maddelerdir (ester oluşumunu gösteren aşağıdaki resme bakın).
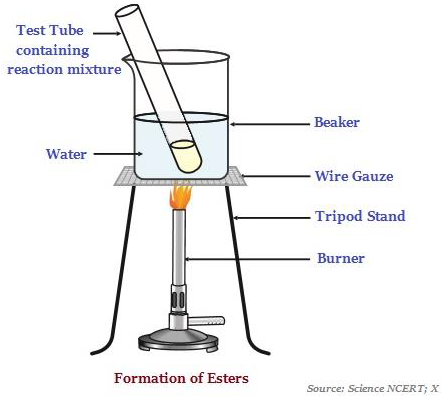
Esterler bir asit veya baz varlığında reaksiyona girdiğinde alkol ve karboksilik asidi geri verir.
Esterlerin bir asit veya bir baz ile reaksiyona girmesi, saponification çünkü sabun yapımında kullanılmaktadır.
Sabun molekülleri normal olarak uzun zincirli karboksilik asitlerin sodyum veya potasyum tuzlarıdır.
İlginç bir şekilde, sabunun iyonik ucu suda çözünür, karbon zinciri ise yağda çözünür. Sabun moleküllerinin bu tipik özellikleri olarak bilinen yapıları oluşturur.micelles (aşağıda verilen resme bakın)

Misellerde moleküllerin bir ucu yağ damlacığına doğru iken iyonik uç dışarıda kalır.
Sabun misel, kirin suda çözülmesine yardımcı olur; aynı şekilde giysiler temizlenir.
Öte yandan, deterjanlar genellikle uzun zincirli karboksilik asitlerin amonyum veya sülfonat tuzlarıdır ve sert suda bile etkili kalır.
Deterjanlar, şampuan ve diğer bazı ürünlerin temizliğinde geleneksel olarak kullanılır.